Brasil deu primeiro passo para regulamentar maconha medicinal; e agora?
A Agência Nacional de Vigilância Sanitária (ANVISA) aprovou por unanimidade nesta terça, 11, as propostas de regulamentação do cultivo de maconha para fins medicinais e científicos, e dos termos para produção, distribuição e comercialização de medicamentos à base da planta. Apenas empresas serão autorizadas a fazer o cultivo.
A Agência Nacional de Vigilância Sanitária (ANVISA) aprovou por unanimidade nesta terça, 11, as propostas de regulamentação do cultivo de maconha para fins medicinais e científicos, e dos termos para produção, distribuição e comercialização de medicamentos à base da planta. Apenas empresas serão autorizadas a fazer o cultivo.
A decisão foi publicada no diário oficial nesta sexta, 14, e daqui a 7 dias a sociedade civil terá dois meses para dar suas contribuições e, posteriormente, debatê-las em duas audiências públicas, que devem definir os termos das linhas de ação propostas pelo órgão em sua deliberação.
A regulamentação da cannabis para fins medicinais é pauta da instituição há pelo menos 2 anos, quando foi criada a agenda de trabalho até 2020, em que a maconha aparecia como um dos principais pontos. Essa urgência se deve ao crescente número de pedidos de importações de medicamentos à base da erva.
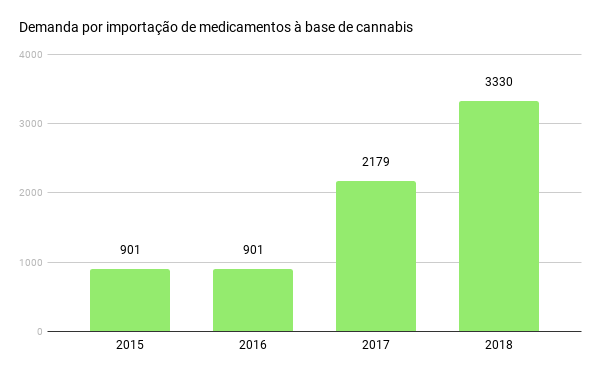
Fonte: Proposta de Consulta Pública / Anvisa
“Mais de 6 mil pessoas pediram importação desses produtos, e a leitura da ANVISA, que ao meu ver é acertada, é que esses produtos importados são caros e de baixa confiabilidade. Então, há interesse da agência em liberar uma produção nacional a partir das empresas que têm interesse”, avalia Renato Filev, doutor em neurologia e neurociências pela Universidade Federal de São Paulo (UNIFESP).
Essa demanda popular, de famílias e instituições, que precisam da maconha para seu uso medicinal, foi o grande propulsor dessa pauta, adiada desde 2017 pela ANVISA, que prometeu naquele ano o início do processo de legalização da erva para uso terapêutico.
“A manutenção da situação atual poderá levar ao agravamento das consequências apresentadas, tais como: judicialização, o aumento da demanda para autorização excepcional de importação de produtos e a dificuldade de acesso a produtos registrados”, salienta na proposta.
Foram muitos anos de luta para que em 2015 o órgão tomasse a primeira medida nessa direção, quando aceitou a importação de medicamentos com o princípio ativo canabidiol, e dois anos depois o primeiro remédio, o Mevatyl.
Os preços desses remédios, no entanto, são impraticáveis para a maioria dos brasileiros, chegam a mais de 2 mil reais por mês em alguns casos. Estratégias como a judicialização de casos para cultivo caseiro através de habeas corpus preventivo não são incomuns, pois tornaram-se uma medida eficiente para quem necessita do tratamento.
Com a regulamentação, a agência argumenta que uma produção nacional irá colocar mais produtos no mercado e consequentemente a tendência dos preços é cair, tornando-o mais acessível para a população e gerando uma indústria capaz de atender a crescente exigência, em sua maior parte de portadores de epilepsia, autismo, dores crônicas, mal de Parkinson e alguns tipos de câncer.
“A ANVISA deve estar ciente do processo histórico que culmina com essa regulamentação do cultivo de cannabis, reconhecendo o protagonismo dos pacientes na introdução desse uso no Brasil e todo o saber que essas pessoas acumularam ao longo do tempo. Antes da ação estatal ou da vontade empresarial, vêm a necessidade das pessoas que usam a cannabis para tratar as mais diversas moléstias, é essa causa humanitária que deve ser guia desse processo regulatório”, aponta Emílio Figueiredo, advogado e consultor jurídico do Growroom, maior fórum de cultivadores do Brasil.
Como vai ser isso?
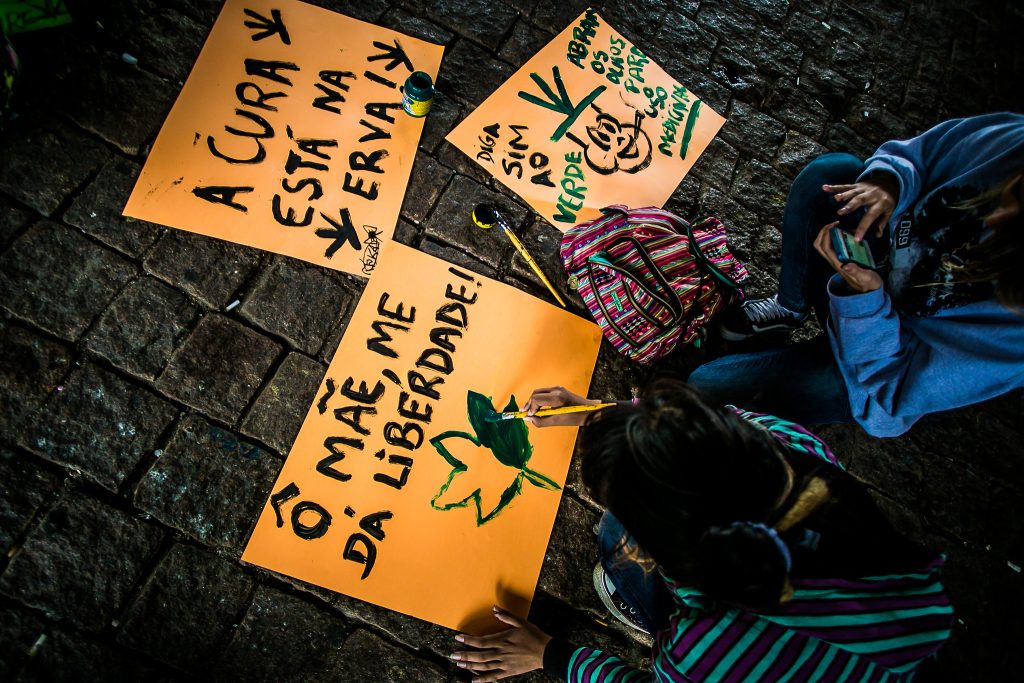
Foto: Mídia NINJA
Vamos aos detalhes: foram duas propostas, chamadas ‘Resoluções da Diretoria Colegiada (RDC), 1) regulamentação do cultivo para uso medicinal e científico; 2) registro, procedimentos e monitoramento de medicamentos. A cúpula, que votou favorável por unanimidade, é formada por 4 pessoas, em que cabe a presidência à William Dib, responsável pela relatoria da votação.
Dib já havia antecipado à Folha de S.Paulo os pontos do processo, dando a principal informação que cultivadores brasileiros, hoje na ilegalidade, esperavam saber: a regulamentação é para quem? A resposta é: grandes empresas.
Conforme dito anteriormente, desde 2017 a agência se debruça sobre esse tema e formou-se um grupo técnico para analisar qual seria o modelo da regulamentação brasileira da erva. Os especialistas viajaram para 4 países em que há mercado legal de maconha medicinal: EUA, Canadá, Israel e Portugal.
“No Canadá, eu mesmo tive a honra de visitar algumas facilities de produção, com cultivos indoor e em greenhouse e ver com meus próprios olhos as reações dos técnicos aos locais e processos. (…) Por tudo que vivenciei na época, apostava que teríamos algo na linha do Canadá, dado a ótima impressão que os sítios de produção das empresas que visitamos deixaram nos técnicos da ANVISA”, narra em artigo o neurocientista e empreendedor, Fabrício Pamplona, em artigo essencial sobre essa história toda.
E foi isso mesmo. O Brasil segue o Canadá em seus primeiros anos de legalização, iniciada em 2001 (triste sacar como estamos atrasados), e dá prioridade para grandes empresas fazerem o cultivo, através da determinação de um conjunto de regras complexas, caras e rígidas para a produção da cannabis.
Determina-se nas resoluções que toda a fabricação deve ser realizada in door, ou seja, em ambiente fechado, apenas por pessoa jurídica. A venda só pode ser feita para instituições de pesquisa, fabricantes de insumos farmacêuticos e medicamentos, e fica vetado para pessoa física, distribuidoras e farmácia de manipulação.
Além disso, haverá um rígido monitoramento de toda a produção, desde o plantio, até a colheita, secagem, embalagem, armazenamento e venda. E mais, como uma espécie de “RG”, que tenha rastreabilidade do produto do produtor ao transportador, drogaria e paciente.
Como assegurar isso? “É conta de matemática”, garante Dib para a Folha. “Haverá cotas de produção e, com base nisso, eu sei que ali produzimos mil caixinhas. Com isso, ou tenho mil receitas, ou tenho alguém preso”.
O plano de segurança será duro e cada aspecto, mesmo os básicos, serão inspecionados pela ANVISA, como planta arquitetônica, proteção ambiental, antecedentes criminais dos trabalhadores, não pode haver identificação da empresa, acesso ao local somente com sistema biométrico, portas e janelas duplas, materiais da construção do prédio reforçados e monitoramento por vídeo 24h, 7 dias por semana.
Não terá venda da planta em si, nem de outros produtos, fica restrita a medicamentos na forma de cápsula, comprimido, pó, líquido e solução, somente para pessoas com doença grave, debilitante, sob ameaça de vida e sem nenhuma outra alternativa terapêutica. Dib ainda salientou, a fim de evitar conflitos com os atuais políticos conservadores que estão no poder, de que não está liberando a planta, mas sim medicamentos com sua composição.
De passagem: maconha no Brasil é realmente um perigo, é preciso um prédio nos moldes de prisão federal para cultivar um remédio.
E para pesquisar vai valer?
Para pesquisa, os requisitos de segurança são os mesmos, acrescidos de autorização da agência, projetos específicos com 2 anos de duração, passível de renovação, e relatórios trimestrais.
“Para pesquisar você vai precisar de investimentos de agências de financiamento públicas, que na situação atual do Brasil é possível que não haja interesse. Com isso, é possível que para a universidade realizar pesquisas tenha que ter incentivo de alguma parceria público privada, que acaba sendo atrelado a uma diminuição da capacidade de pesquisa”, aponta Filev.
“Essas pesquisas, em geral, vão ficar voltadas para interesses de regulação, de registros desses medicamentos, mas para uma abrangência maior, em áreas básicas, como psicofarmacológicas, agronomia e botânica, fica mais mais difícil”, completa o pesquisador.
Que mercado é esse?
Como mencionado no início, há uma demanda de pelo menos 6 mil pessoas importando medicamentos do exterior, mas a capacidade desse mercado alcança cifras de fazer inveja e atiçar a cobiça de muitos investidores que, com o passo dado pela ANVISA essa semana, já cresceram os olhos para o Brasil e abriram as carteiras.
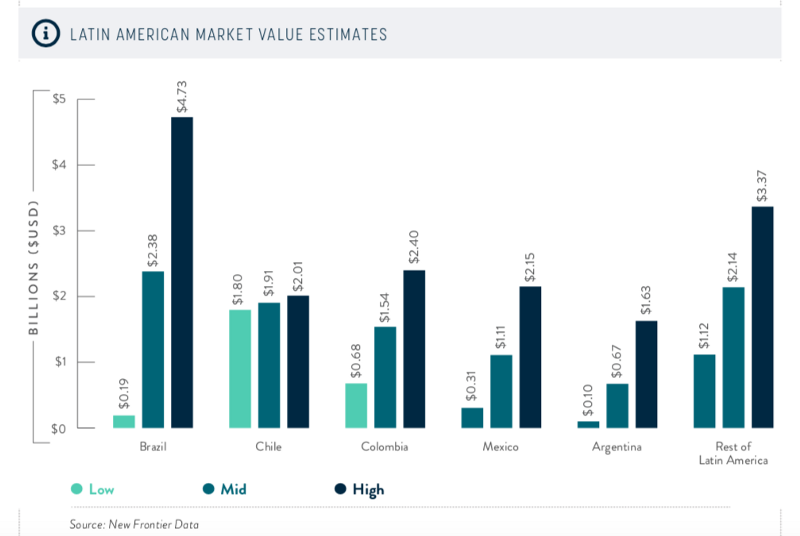
Gráfico retirado do artigo “Um mercado regulado para os grandes”, de Fabrício Pamplona, já citado nesse texto.
Com potencial para alcançar quase 5 bilhões de dólares no país, esse mercado já vem fazendo bilionários em todo o mundo e agora vê por aqui uma nova oportunidade de fabricar mais dinheiro.
Um dia após a decisão da agência, a empresa canadense Canopy Growth anunciou que fará um investimento de 60 milhões de reais em terras tupiniquins, com promessa de expansão para 150 milhões no futuro, através do seu braço farmacêutico, a Spectrum Therapeutics. A organização já tem investimentos na Colômbia, vizinho que está à nossa frente na regulamentação da cannabis medicinal.
E o governo com isso?

Foto: Mídia NINJA
Já sabemos que o governo Bolsonaro não é o mais simpático a qualquer tipo de flexibilização em relação às drogas ilícitas, ao contrário, em seu pouco tempo de presidência, já está marcado pelo endurecimento da lei de drogas, através do seu Ministro de Cidadania, Osmar Terra, autor das proposições que, entre outras coisas, passa a facilitar internações compulsórias de usuários de drogas e aumenta a pena para crime de tráfico.
Nessa toada, ele não deixou barato. Terra chamou a ANVISA de irresponsável e que a está indo “contra a lei, contra as evidências científicas e contra o Congresso e o Governo Brasileiro”. Sua opinião foi seguida pelo Conselho Nacional de Medicina (CNM) e pela Associação Brasileira de Psiquiatria (ABP), que alertaram para “o alto risco envolvido nessa ação”. De acordo com as organizações, “o uso de Cannabis sativa L. in natura e seus derivados não garantem efetividade e segurança para seus pacientes”. Apesar disso, a CNM aprovou em 2014 a indicação de CBD para crianças com epilepsia. Vai entender.
Além disso, a repórter Natália Cancian, da Folha de S.Paulo, noticia no podcast Café da Manhã desta quinta-feira, 13, que apesar do caráter independente da agência, ou seja, imune à qualquer intervenção do governo, em breve uma cadeira da diretoria da ANVISA deve estar vaga e Bolsonaro deve nomear um novo nome, que, se alinhado aos seus interesses, pode pedir vistas do processo e adiar ainda mais sua tramitação.
